Данас разликујемо четири нивоа организације у структури протеина. Оне су резултат веома сложених структурних односа. То су:
1) Примарна структура протеина
2) Секундарна структура протеина
3) Терцијарна структура протеина
4) Кватернерна структура протеина
Примарна структура протеина
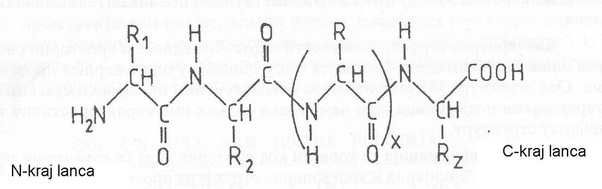
Примарна структура протеина подразумева секвенцу, односно број, врсту и редослед аминокиселина у полипептидном ланцу. Она је у потпуности одређена генима. Такође, примарну структуру одликује структурна повезаност ковалентним пептидним везама (то су амидне функционалне групе), које су настале током процеса транслације. На једном крају полипептидног ланца налази се слободна -NH2 група прве аминокиселине у низу, и он се зато назива N – крај, док се слободна –COOH група налази на другом крају који припада последњој аминокиселини у низу, и он се означава као C – крај.
1) Примарна структура протеина
2) Секундарна структура протеина
3) Терцијарна структура протеина
4) Кватернерна структура протеина
Примарна структура протеина
Примарна структура протеина подразумева секвенцу, односно број, врсту и редослед аминокиселина у полипептидном ланцу. Она је у потпуности одређена генима. Такође, примарну структуру одликује структурна повезаност ковалентним пептидним везама (то су амидне функционалне групе), које су настале током процеса транслације. На једном крају полипептидног ланца налази се слободна -NH2 група прве аминокиселине у низу, и он се зато назива N – крај, док се слободна –COOH група налази на другом крају који припада последњој аминокиселини у низу, и он се означава као C – крај.
Секундарна структура протеина
Секундарна структура протеина означава правилан распоред полипептидног ланца дуж једне осе. Она је локално дефинисана. То значи да у једном молекулу протеина могу постојати различити облици ове структуре.
Стабилност секундарне структуре постигнута је постојањем водоничних веза. Различите аминокиселине се разликују по својој способности формирања разних елемената секундарне структуре.
Најчешћи облици секундарне структуре, а истовремено и најстабилнији су:
· α – завојница (α – helix)
· β – конформација(β – плоча)
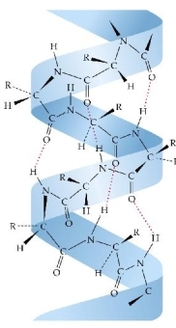
α – helix настаје увијањем полипептидног ланца око покретљивих веза у смеру казаљке на сату. У оваквој структури, сваки спирални навој садржи 3,6 остатака аминокиселина. Између атома који припадају свакој четвртој аминокиселини у полипептидном ланцу образују се водоничне везе. Оне се успостављају између карбонилног кисеоника (C=O) једног аминокиселинског остатка и N-H водоника четврте аминокиселине у низу. На тај начин, све пептидне везе учествују у формирању водоничних веза, па због њиховог великог броја ова структура стабилна.
У β – плочи, за разлику од α – helixа, ланац није спирализован, већ је издужен. У њему се полипептидни ланци пружају “цикцак“ , тј. антипаралелни су. Водоничне везе одржавају и ову структуру, образујући се између удаљених делова истог полипептидног ланца.
Као и α – helix, и β – плоча припада фибриларним протеинима, само је у питању другачија конформација.
Секундарна структура протеина означава правилан распоред полипептидног ланца дуж једне осе. Она је локално дефинисана. То значи да у једном молекулу протеина могу постојати различити облици ове структуре.
Стабилност секундарне структуре постигнута је постојањем водоничних веза. Различите аминокиселине се разликују по својој способности формирања разних елемената секундарне структуре.
Најчешћи облици секундарне структуре, а истовремено и најстабилнији су:
· α – завојница (α – helix)
· β – конформација(β – плоча)
α – helix настаје увијањем полипептидног ланца око покретљивих веза у смеру казаљке на сату. У оваквој структури, сваки спирални навој садржи 3,6 остатака аминокиселина. Између атома који припадају свакој четвртој аминокиселини у полипептидном ланцу образују се водоничне везе. Оне се успостављају између карбонилног кисеоника (C=O) једног аминокиселинског остатка и N-H водоника четврте аминокиселине у низу. На тај начин, све пептидне везе учествују у формирању водоничних веза, па због њиховог великог броја ова структура стабилна.
У β – плочи, за разлику од α – helixа, ланац није спирализован, већ је издужен. У њему се полипептидни ланци пружају “цикцак“ , тј. антипаралелни су. Водоничне везе одржавају и ову структуру, образујући се између удаљених делова истог полипептидног ланца.
Као и α – helix, и β – плоча припада фибриларним протеинима, само је у питању другачија конформација.
Терцијарна структура протеина
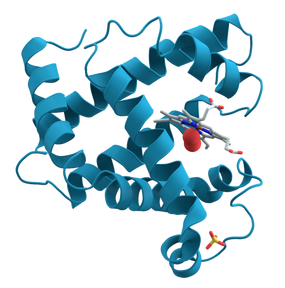
Терцијарна структура је тродимензионална структура појединачног молекула протеина. Она се односи на начин увијања и савијања полипептидног ланца у простору. Терцијарна структура је у великој мери одређена примарном структуром протеина. Методе које користе примарну структуру за предвиђање терцијарне су опште познате као методе предвиђања протеинске структуре.
Поред водоничних веза, ова структура је стабилизована још и интрамолекулским јонским, хидрофобним и дисулфидним везама, оствареним између функционалних група из бочних низова аминокиселина.
Терцијарна структура је тродимензионална структура појединачног молекула протеина. Она се односи на начин увијања и савијања полипептидног ланца у простору. Терцијарна структура је у великој мери одређена примарном структуром протеина. Методе које користе примарну структуру за предвиђање терцијарне су опште познате као методе предвиђања протеинске структуре.
Поред водоничних веза, ова структура је стабилизована још и интрамолекулским јонским, хидрофобним и дисулфидним везама, оствареним између функционалних група из бочних низова аминокиселина.
Кватернерна структура протеина
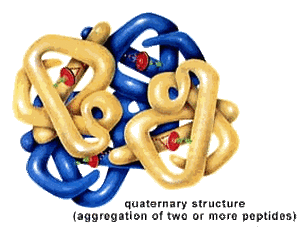
Већина протеина се састоји од више полипептидних ланаца. Кватернерна структура обухвата просторни распоред и међусобне односе више полипептидних ланаца у протеинима. Ове, као и терцијарне структуре обично се називају “конформације“ , а прелази између њих су конформационе промене.
Појединачни полипептидни ланци називају се подјединице, а део олигомера са одређеном билошком улогом назива се субјединица. Њу може да чини само један полипептидни ланац, а може је чинити и неколико њих. Број подјединица у олигомерним комплексима описује се коришћењем назива који се завршава на –мер. На пример, протеин са две подјединице називамо димер, протеин са три подјединице тример, а протеин са четири подјединице тетрамер. Кватернерна структура је стабилизована истим бројем интеракција као и терцијарна структура. Те интеракције су нековалентне интермолекулске везе подјединица, при чему свака од њих има карактеристичну терцијарну структуру.
Већина протеина се састоји од више полипептидних ланаца. Кватернерна структура обухвата просторни распоред и међусобне односе више полипептидних ланаца у протеинима. Ове, као и терцијарне структуре обично се називају “конформације“ , а прелази између њих су конформационе промене.
Појединачни полипептидни ланци називају се подјединице, а део олигомера са одређеном билошком улогом назива се субјединица. Њу може да чини само један полипептидни ланац, а може је чинити и неколико њих. Број подјединица у олигомерним комплексима описује се коришћењем назива који се завршава на –мер. На пример, протеин са две подјединице називамо димер, протеин са три подјединице тример, а протеин са четири подјединице тетрамер. Кватернерна структура је стабилизована истим бројем интеракција као и терцијарна структура. Те интеракције су нековалентне интермолекулске везе подјединица, при чему свака од њих има карактеристичну терцијарну структуру.